هل فكرت يومًا كيف يمكن الحصول على المياه العذبة من مياه البحر؟ أو كيف يمكننا الحصول على الحليب خالي من الدسم؟ أو كيف يتم فصل الدم إلى مكوناته الأربعة في المستشفيات وبنوك الدم؟
الرمل والماء / الحبوب والحليب / السكر والملح / الملح والماء / الماء والإيثانول / الماء والفلفل / الأسمنت / الدم ، كل هذه أمثلة على المخاليط التي يمكن فصلها بالطرق الفيزيائية. يمكننا ان نجد العديد من الأمثلة على المخاليط من حولنا في حياتنا اليومية.
في هذا المقال، سنناقش المخاليط وأنواعها وخصائها وكذلك سنتعرف على أشهر تقنيات فصل المخاليط.
ما المقصود بالمخاليط؟

المخاليط هي المواد التي تتكون من مكونان أو أكثر من المواد التي لا تتحد أو تختلط معًا بالطرق الكيميائية (لا تحدث تفاعلات كيميائية بين المكونات). ويمكننا القول أن أي مادة ليست خليطًا هي مادة نقية.
إذا نظرت حولك ستجد العديد من الأمثلة على المخاليط مثل الهواء الذي نتنفسه والمحيطات والبحار والأنهار؛ فمياه البحار والمحيطات هي خليط من الملح والمياه الطبيعية والمعادن الأخرى. الهواء عبارة عن خليط من الغازات مثل الأكسجين و ثاني أكسيد الكربون والنيتروجين وغيرهم.
الخاصية الأكثر تمييزًا للمخاليط هي القدرة على فصل كل مكون بسهولة بالطرق الفيزيائية ودون أي تغييرات كيميائية. تحتفظ كل مادة أو مكون بخصائصه الكيميائية والفيزيائية الفردية دون أي تغييرات.
إذن، يمكننا القول إن عملية فصل المخاليط هي مجرد عملية مزج ميكانيكية؛ لأن كل مكون لا يشارك في أي روابط كيميائية.
أشهر أنواع المخاليط
هناك العديد من أنواع المخاليط، ولكل نوع خصائصه الفريدة:
-
الغروي
في الخليط الغروي، تكون الجسيمات صغيرة جدًا بحيث لا يمكن فصلها عن المحلول عن طريق الترشيح أو الطرد المركزي. تتكون هذه المخاليط عادة من مادتين أو أكثر مذابة في مذيب سائل. بعض الأمثلة على المخاليط الغروية هي الحليب والجيلاتين والطلاء والماء.
-
المحلول
في خليط المحلول، لا تذوب المواد تمامًا في المذيب السائل. بدلا من ذلك، فإنها تشكل جزيئات صغيرة معلقة في السائل. نتيجة لذلك يمكن فصل هذه الحلول عن طريق الترشيح أو الطرد المركزي. ومن أمثلة مخاليط المحاليل الماء مع السكر والملح والخل والزيت والدم والبلازم
-
المعلق
في خليط المعلق، يتم توزيع المواد بالتساوي في جميع أنحاء المذيب السائل. نتيجة لذلك، يمكن فصل المعلق بسهولة عن طريق الترشيح أو الطرد المركزي. أمثلة على المخاليط المعلقة معجون الأسنان والخرسانة والطين.
-
المستحلب
في خليط المستحلب، يتم توزيع المادتين بالتساوي في جميع أنحاء المذيب السائل، لكن السوائل لا تختلط تمامًا. نتيجة لذلك يمكن فصل الخليط إلى قسمين عن طريق إضافة كمية صغيرة من السائل إلى المذيب. أمثلة على مخاليط المستحلب هي الشامبو والمايونيز.
قبل الحديث عن فصل المخاليط نريد أن نتأكد من معرفتك بخصائص المخاليط التالية:
- مكونات الخليط من مادتين أو أكثر يمكن أن تكون غير متجانسة أو متجانسة في الطبيعة.
- لا توجد قوة تؤثر بين مواد الخليط.
- تحدد خصائص كل مكون أو مادة خصائص الخليط بأكمله.
- يتم استخدام الطرق الفيزيائية فقط لفصل المخاليط إلى موادها الفردية الذائبة.
- يتم تحديد خصائص الخليط مثل درجة الانصهار ونقطة الغليان من خلال خصائص المواد الفردية (نقاط الانصهار والغليان).
- يمكن أن تتحد المواد أو المواد الموجودة في الحالة الصلبة أو السائلة أو الغازية معا وتشكل الخليط.
- أثناء تكوين الخليط، لا يوجد تغيير في الطاقة.
- تحتفظ كل مادة فردية من الخليط بخصائصها الكيميائية والفيزيائية الأصلية دون أي تغييرات.
- يمكن العثور على كل مكون من مكونات الخليط بأي نسبة (تختلف النسب).
فصل المخاليط

عادة ما يكون فصل المخاليط أسهل من فصل المواد النقية. تخيل أن بعض المسامير قد أُسقطت في حفرة رملية لطفل وغرقت في الرمال بحيث لا يمكن رؤيتها. تتمثل إحدى طرق فصلها عن الرمال في استخدام مغناطيس، لأنه ينجذب إلى الحديد. يعمل هذا لأن المسامير والرمل لهما خصائص أو ميزات مختلفة – ينجذب الحديد إلى المغناطيس ، لكن الرمل ليس كذلك.
مثال آخر لمزيد من فهم ما هو “فصل المخاليط”:
لا يمكن فصل الخرز البلاستيكي والرمل بمغناطيس. مفتاح فصلها هو التعرف على الخصائص المختلفة للخرز البلاستيكي والرمل. الفرق الواضح هو الحجم. الخرزات البلاستيكية أكبر بكثير من حبيبات الرمل. هناغربال رمل بسيط سيفي بالغرض.
طرق فصل المخاليط
نظرا لأن أي خليط يميل إلى أن يأتي بأشكال مختلفة، يقوم العلماء بإنشاء عدة طرق لفصل الخليط من المواد إلى مكوناته الفردية والغرض المهم الآخر لفصل المخاليط هو إزالة المواد غير المرغوب فيها والحصول على المكونات المفيدة والمطلوبة فقط.
يمكن فصل المخاليط باستخدام العديد من الطرق التالية:
- الترشيح
- التقطير
- التكثيف
- المغناطيسية
- الفصل اللوني
ملاحظة: هناك العديد من طرق فصل الخلطات التي نستخدمها في حياتنا اليومية مثل القطف باليد والغربلة والدرس.
فصل المخاليط بالترشيح
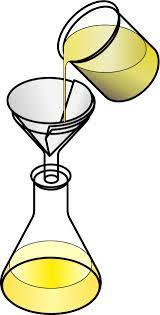
الترشيح من طرق فصل المخاليط التي تستخدم بشكل أساسي لفصل مكونات المخاليط التي تحتوي على مادة صلبة غير منفصلة في سائل. يمكن استخدامه أيضا لإزالة الشوائب من الخليط. يتضمن الترشيح استخدام نوع من المواد التي تفصل بين المواد المختلفة. يمكن إجراء الترشيح بعدة طرق اعتمادًا على المادة التي تحاول فصلها والمواد التي تستخدمها.
يعد الترشيح هو الطريقة الأكثر شيوعا لفصل المادة الصلبة غير القابلة للذوبان عن السائل.
يمكن إجراء عملية فصل المخاليط بالترشيح من خلال العديد من التقنيات (حسب الغرض من الترشيح) مثل طريقة القمع الزجاجي البسيط / طريقة قمع بوشنر / باستخدام طريقة الجاذبية / باستخدام طريقة التفريغ.
لذلك يمكننا القول أن الترشيح هو عملية فصل خليط سائل عن طريق تدفقه عبر وسط مرشح يحتفظ بجزيئات أصغر من فتحات المرشح وهذا يختلف عن التبخر في أن السائل يظل سائلًا أثناء الترشيح.
أمثلة على فصل المخاليط بالترشيح
يمكننا القول أن طريقة الترشيح من طرق فصل السوائل ذات الكثافات المختلفة باستخدام وسائل ترشيح مختلفة. على سبيل المثال، في معالجة مياه الصرف الصحي، يتم تصفية المياه والمواد العضوية باستخدام مرشحات مختلفة.
في صناعة الأدوية، يتم فصل الزيوت والجزيئات الصلبة عن السوائل المعتمدة على الماء من خلال استخدام نظام الترشيح. الزيت والماء كلاهما غير قابل للامتزاج ، مما يعني أنه لا يمكن خلطهما بحرية مع بعضهما البعض. يؤدي هذا إلى غرق الزيت في قاع أي حاوية يتم وضعه فيها ، بينما يبقى الماء في الأعلى. أثناء الترشيح ، يغرق الزيت الأكثر كثافة في القاع ويرتفع الماء الأخف إلى الأعلى. بعد ذلك ، يستمر الفصل من خلال أنبوب في قاع الحاوية حيث يتدفق الماء أثناء الاحتفاظ بالزيت في الحاوية. وتسمى هذه العملية الترشيح بالجاذبية.
مثال آخر على الترشيح في فصل المخاليط في حياتنا اليومية هو استخدام مرشحات القهوة أو أكياس الشاي. يعد ترشيح الخليط المصنوع من الرمل والماء مثالًا أيضًا على الترشيح.
أنواع المخاليط التي يمكن فصلها عن طريق الترشيح:
- خليط صلب مع سائل
- خليط صلب مع صلب
- خليط صلب مع غاز
يوضح الفيديو التالي تجربة فصل المخاليط بالترشيح بالتفصيل
براكسيلابس هي أفضل منصة لمحاكاة تجارب العلوم الافتراضية في الفيزياء والكيمياء والبيولوجيا. أنشئ حسابك المجاني الآن
كيف يمكن فصل المخاليط بالتقطير؟
التقطير هو تقنية فصل المخاليط التي تستخدم بشكل أساسي لاستخراج خليط من المواد الصلبة موجود في سائل. التقطير مناسب في حالة استخراج كل من السوائل والمواد الصلبة من المحلول. التقطير البسيط هو الطريقة التي تعتمد على الاختلافات بين ضغط البخار المقابلة والتقلب الموجودة في مكونات الخليط.
أكثر 4 أنواع شيوعًا من تقنيات فصل المخاليط بالتقطير هي التقطير البسيط والتقطير بالبخار والتقطير التجزيئي والتقطير الفراغي.
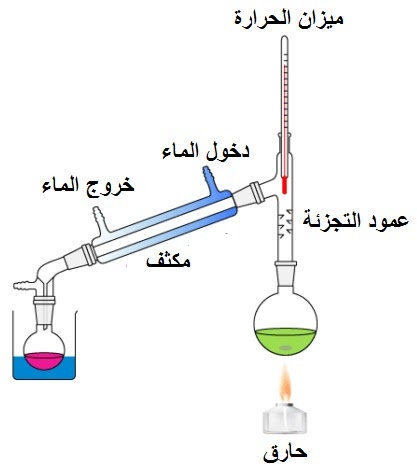
وللإجابة عن سؤال كيف يمكن فصل المخاليط بالتقطير البسيط، سنوضح الخطوات التالية:
أولا، يتم تسخين الخليط السائل بهدف تكوين الأبخرة.
ثم تكثيف الأبخرة الناتجة الثمينة لاستعادة سائل جديد. يعرف هذا السائل الجديد الذي يتم الحصول عليه عن طريق عملية التكثيف باسم ناتج التقطير.
ملاحظة: هناك نوعان من السوائل (السوائل القابلة للامتزاج او المتجانسة والسوائل غير القابلة للامتزاج أو غير المتجانسة).
في المادة القابلة للامتزاج، تختلط السوائل معًا وتشكل محلولًا (على سبيل المثال: الإيثانول والماء). ولكن في حالة السوائل غير القابلة للامتزاج، لا تختلط السوائل جيدًا معًا مثل مزيج الزيت والماء.
تستخدم طريقة فصل المخاليك بالتقطير لفصل السوائل القابلة للامتزاج (المخاليط المتجانسة) والتي لها فرق كاف في درجات غليانها ويمكن غليها دون تحلل.
إذن، يمكننا القول إن التقطير طريقة فصل تستخدم لاستخلاص خليط من المركبات في الحالة الصلبة الموجودة في سائل. يتضمن تسخين عينة سائلة عند ضغط ثابت فيما يتعلق بنقطة غليانها، حتى يتم غلي جميع مكوناتها أو تكثيفها.
أي المخاليط يسهل فصل بعضها عن بعض؟

تعد المحاليل المتجانسة من أكثر انواع المخاليط التي يسهل فصل بعضها عن بعض؛ فمثلا محلول الملح (ماء وملح ) يمكن فصل مكوناته بسهولة عن طريق التبخر مع احتفاظ كل مادة منهما بخصائصها الأصلية.
ما هي أشهر طرق فصل المخاليط المتجانسة؟
الخليط المتجانس هو خليط سائل أو صلب أو غازي يتميز بأن له نفس نسب مكوناته في عينة معينة وهو موحد في التكوين دائمًا.
أشهر الطرق المستخدمة لفصل المخاليط المتجانسة هي التقطير و الفصل اللوني والتبخر.
تجربة فصل المخاليط من براكسيلابس

طريقة الكروماتوغرافيا السائلة عالية الأداء (HPLC) هو طريقة تحليلية تفصل المركبات في المخاليط وتحددها وتحدد كمياتها.
يستخدم HPLC عمود كروماتوغرافيا سائل عالي الأداء لفصل العينات. تحتوي الأعمدة على مرحلة ثابتة من الجسيمات الثابتة، وعادة ما تكون جزيئات هلام السيليكا أو مادة بوليمرية مطلية بالسيلان أو بعض المواد الكيميائية المماثلة. يتدفق الطور المتحرك عبر العمود بمعدل ثابت ويحمل مكونات العينة بعيدا عن منفذ الحقن إلى العمود المليء بالجسيمات.
مثل جميع تقنيات الكروماتوغرافيا السائلة، يمكن لـ HPLC فصل المركبات باستخدام أنواع مختلفة من التفاعلات بين التحليلات والمراحل الثابتة.
توفر براكسيلابس تجربة الكروماتوغرافيا السائلة عالية الأداء high-performance liquid chromatography (HPLC) والتي تعتبر مثالًا على فصل المخاليط في المختبر الافتراضي.
تستخدم تجربة الكروماتوغرافيا السائلة عالية الأداء من براكسيلابس في فصل واكتشاف الأحماض الأمينية في الأنسجة.
تم تصميم هذا الخليط المنفصل الافتراضي لتوفير فهم أساسي لمبدأ وتطبيقات الكروماتوغرافيا السائلة عالية الأداء (HPLC). المحاكاة مخصصة للطلاب الذين لديهم معرفة سابقة قليلة أو معدومة بهذه التقنية. خلال التجربة سيتم تغطية النقاط التالية:
- النظرية والمبادئ الأساسية ل HPLC.
- إعداد مرحلة متنقلة.
- تحضير محلول عينة ل HPLC.
- استخدام أعمدة استبعاد الحجم في HPLC.
- اشتقاق / حقن العينة عن طريق إجراء OPA / FMOC عبر الإنترنت.
توفر معامل براكسيلابس الإفتراضية معمل العلوم الإفتراضي لتجربة (الفصل الكروماتوجرافي الإنجذابي و الفصل الكروماتوجرافي عالي الكفاءة للبروتين) مما يسمح لك بإجراء التجربة بأكملها بسهولة ووضوح مع مقاطع فيديو مبسطة لشرح خطوات العمل، وملفات PDF لشرح المادة العلمية النظرية للتجربة.
 براكسيلابس المدونة العربية لمعامل العلوم الإفتراضية براكسيلابس
براكسيلابس المدونة العربية لمعامل العلوم الإفتراضية براكسيلابس

